
【Cell】新發現:檢查點分子有望成為腫瘤免疫治療的新靶點
發布時間:
2020-09-12 09:00
來源:
免疫療法激活了人體自身對腫瘤的防御,徹底改變了癌癥的療法。然而,盡管免疫療法取得了一些突破性的成功,但只有一小部分患者受益于現有的藥物。
??近日,德國癌癥研究中心(DKFZ)和柏林健康研究所(BIH)的一組研究人員發布了新的數據,研究了腫瘤逃避免疫系統破壞的分子機制,強調了癌癥免疫療法的一個潛在新靶點。科學家們發現,代謝酶IL4I1(白細胞介素-4誘導-1)促進了腫瘤細胞的擴散,并抑制了免疫系統。這種激活二惡英受體的酶在腫瘤細胞大量產生。
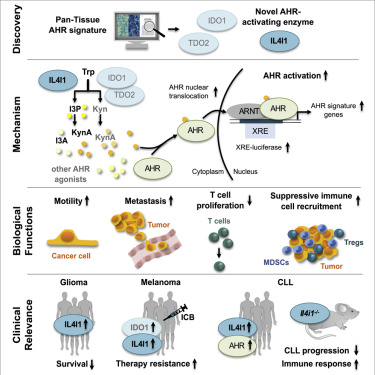
??圖解摘要
??該研究在8月19日發表在《細胞》雜志上,題為“IL4I1 is a Metabolic Immune Checkpoint that Activates the AHR and Promotes Tumor Progression”。

??芳香烴受體(AHR)也被稱為二惡英受體,因為它介導二惡英的毒性作用。然而,不僅是毒素,身體的代謝產物也能激活受體。其中一個例子就是色氨酸的降解產物,色氨酸是我們在食物中攝入的蛋白質的組成部分。腫瘤利用這些代謝物的優勢:它們促進癌細胞的移動性,削弱對腫瘤的免疫反應。
??有一種分子特別引起了科學家的注意:IL4I1酶。波黑分子流行病學的研究小組副組長、該研究的合著者薩斯基亞·特朗普(Saskia Trump)博士解釋說:“IL4I1形成的代謝產物與二惡英受體結合并激活二惡英受體,從而導致免疫細胞受到抑制。”
??研究人員表示,“由色氨酸(Trp)分解代謝物激活的AHR增強了腫瘤的惡性程度,并抑制了抗腫瘤免疫。”
??迄今為止,AHR靶基因的背景特異性阻礙了AHR活性及其上游酶在人類癌癥中的系統研究。通過自然語言處理獲得的一種全組織AHR簽名顯示,在32個腫瘤實體中,IL4I1與IDR1或TDO2的結合頻率高于ATO活性,IDO1或TDO2迄今被認為是主要的Trp分解酶。 IL4I1通過生成吲哚代謝產物和尿酸來激活AHR。它與神經膠質瘤患者的生存期縮短,促進癌細胞運動并抑制適應性免疫有關,從而增強了小鼠慢性淋巴細胞性白血病(CLL)的進展。”
??臨床研究發現,當酶在膠質瘤(一種惡性腦瘤)中濃度較高時,患者的生存幾率降低。此外,在慢性淋巴白血病(CLL)的小鼠模型中,一種血癌IL4I1通過其對免疫系統的影響被證明可以促進癌癥的發生。
??DKFZ的團隊領導、該研究的合著者Martina Seiffert博士表示,“在那些由于基因改變而在腫瘤環境中不產生IL4I1的動物中,免疫系統在阻止癌癥進展方面明顯更成功。”
??DKFZ的組長,高級研究員Christiane Opitz博士總結說:“IL4I1有很大潛力成為藥物的靶點。到目前為止,抑制色氨酸代謝酶的藥物在臨床試驗中都失敗了,因為腫瘤對它們沒有反應。然而,IL4I1的作用到目前為止被忽視了,這種酶作為一個目標分子還沒有被測試。”
??參考:
【1】https://www.genengnews.com/news/checkpoint-molecule-could-be-new-cancer-immunotherapy-target/
【2】https://www.cell.com/cell/fulltext/S0092-8674(20)30946-6
