
近年來,腫瘤免疫治療越來越受到重視,但許多患者的腫瘤仍不能對現有的免疫治療方法產生反應。激活干擾素基因(STING)通路的刺激因子,可以促進腫瘤微環境中的免疫反應,但缺點是需要多次瘤內注射,這對許多腫瘤是不現實的。對此,科學家最近開發出了一種工程化微粒,可在腫瘤中注射一次后緩慢釋放激動劑,并在多種腫瘤模型中顯示了良好的效果。
發布時間:
2020-08-18 09:00
來源:

TMBIM6是內質網(ER)應激的抑制劑,最初命名為BAX抑制劑(BI)-12。BI-1/TMBIM6是含蛋白3家族跨膜BI-1基序的成員。TMBIM6是一種鈣離子通道樣蛋白,可降低內質網ER膜表面表達的鈣離子穩態。它在許多癌癥類型中上調,包括乳腺癌、肺癌、前列腺癌、鼻咽癌和肝癌。
??在之前的研究中,TMBIM6的過度表達通過調節細胞的流動性和侵襲性以及葡萄糖代謝來促進腫瘤轉移。抑制TMBIM6會導致細胞死亡,從而減少腫瘤的發生。最近,研究人員報道了Sp1和PKC調節TMBIM68的轉錄表達。PKC在各種癌癥類型中也有高表達,如在肝癌、前列腺癌和乳腺癌中。盡管許多證據支持TMBIM6參與了多種癌癥的發生,但TMBIM6在癌癥進展中作用的分子機制研究較少。
??雷帕霉素(mTOR)的機械靶點在細胞代謝、細胞生長和營養敏感方面起著關鍵作用。mTOR復合物(mTORC)1和mTORC2是兩種結構和功能不同的蛋白質復合物,在癌癥和糖尿病中經常過度表達。
??在本研究中,研究人員確定TMBIM6是mTORC2在ER膜上的主要結合伙伴。這樣的結果為調控AKT的激活和腫瘤發生的mTORC2–TMBIM6核糖體軸提供了證據。
??為了研究TMBIM6在腫瘤進展中的致癌作用,研究人員首先分析了來自NCBI/GEO的多個腫瘤樣本的TMBIM6 mRNA表達譜數據集。這些分析顯示,TMBIM6在纖維肉瘤、宮頸癌、子宮內膜癌和外陰癌、乳腺癌、肺癌和前列腺癌中顯著過度表達。接下來,研究人員用組織微陣列比較了TMBIM6在同一腫瘤組織中的表達水平,也得到了相似的結果。
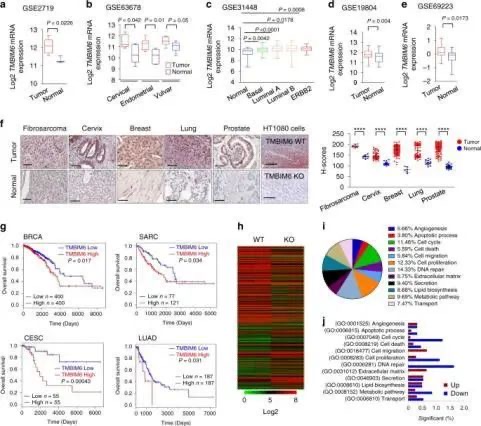
??腫瘤組織中TMBIM6表達增加
??該研究發現,TMBIM6缺失或敲除會抑制原發腫瘤的生長。此外,mTORC2的激活被TMBIM6上調,并刺激糖酵解、蛋白質合成、脂質合成基因和糖基化蛋白的表達。此外,研究人員發現BIA化合物,一種潛在的TMBIM6拮抗劑,可以阻止TMBIM6與mTORC2結合,降低mTORC2活性,還可以調節TMBIM6泄漏的鈣離子,進一步抑制腫瘤的形成和進展。
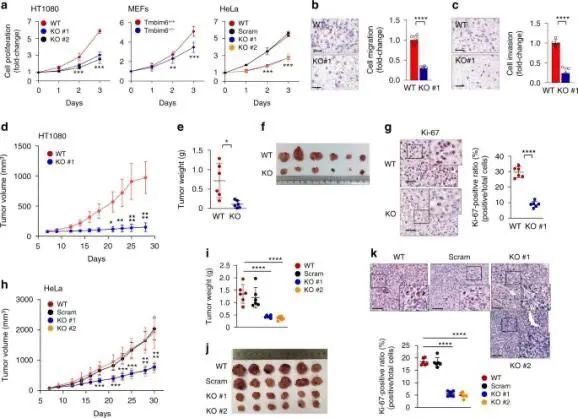
??TMBIM6促進腫瘤生長。
??TMBIM6通過mTORC2核糖體軸激活AKT通路,評價調節WT細胞和TMBIM6-KO-HT1080細胞腫瘤進展的信號蛋白分子。
??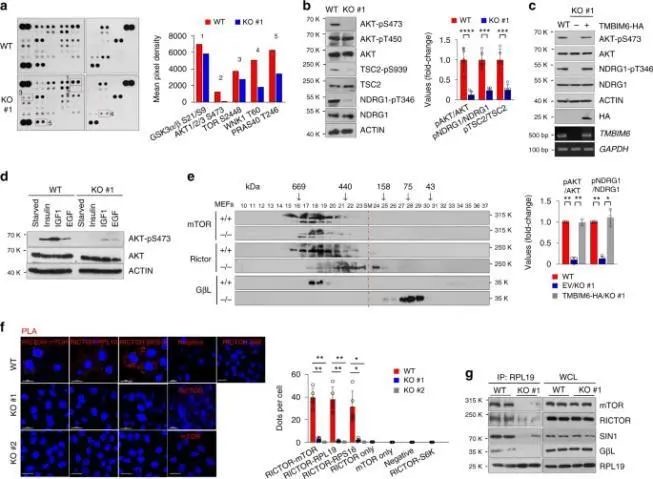
TMBIM6調節mTORC2的激活
??本研究結果顯示,TMBIM6通過直接結合和刺激鈣離子釋放來增強mTORC2的活性和組裝。TMBIM6的破壞限制了原發性腫瘤的生長,并損害了癌細胞的新陳代謝。此外,研究人員還發現小分子化合物BIA是一種潛在的抗癌藥物,可以阻止mTORC2和TMBIM6之間的結合。
??該研究表明,TMBIM6通過調節糖酵解和PPP來調節糖代謝,這對mTORC2的活性和信號傳遞至關重要。鑒于在乳腺癌、前列腺癌、宮頸癌和肺癌中觀察到的TMBIM6上調,由mTORC2介導的代謝變化,尤其是AKT可能是癌癥進展的主要機制。此外,TMBIM6缺失抑制GSH的生物合成,GSH可能更容易受到活性氧和脂質生物合成的影響,從而抑制腫瘤的發生。本研究表明,TMBIM6是調節mTORC2活性和腫瘤細胞生物能量的重要調節因子。
??這些數據表明,TMBIM6作為幾種癌癥疾病預后的預測生物標志物具有潛在的臨床價值。
??參考:https://www.nature.com/articles/s41467-020-17802-4
