
【PNAS】麻醉劑對意識的影響有結論了!一個世紀以來的科學爭論落下了帷幕
發布時間:
2020-06-15 09:00
來源:

如果沒有全身麻醉,手術是不可想象的,因此,盡管有175年的醫療史,醫生和科學家仍然無法解釋麻醉劑是如何使病人暫時失去知覺的。
??在5月28日晚上,斯克里普斯研究所(Scripps Research)的一項新研究發表在《美國國家科學院院刊》(PNAS)上,解決了這個長久以來的醫學謎團。利用現代納米級的顯微技術,再加上在活細胞和果蠅身上進行的巧妙的實驗,科學家們展示了細胞膜中的脂類簇是如何在兩部分機制中充當缺失的中間環節的。短暫麻醉可使脂質A簇從有序狀態轉移到紊亂狀態,然后來回反復,導致大量的后續效應,最終導致意識的改變。

??美國國家科學院院士、曾任斯克里普斯研究院院長的化學家理查德·勒納(Richard Lerner)博士和分子生物學家斯科特·漢森(Scott Hansen)博士的發現解決了一個世紀以來的科學爭論,這個爭論至今仍在醞釀:麻醉劑是直接作用于被稱為離子通道的細胞膜門上,還是以某種方式作用于細胞膜上,以一種新的、出乎意料的方式發出細胞變化的信號?他們兩人表示,經過近五年的實驗、呼吁、辯論和挑戰,終于得出結論:這是一個從膜開始的兩步過程。麻醉劑擾亂了被稱為“脂筏”的細胞膜內有序脂簇,從而啟動了信號。
??勒納說:“我們認為,毫無疑問,這條新的途徑正被用于意識之外的其他大腦功能,使我們現在能夠進一步破解大腦的其他奧秘。”。
??1846年,在波士頓馬薩諸塞州總醫院的一個腫瘤病人身上,乙醚引起意識喪失的能力第一次被證明,當時在一個后來被稱為“乙醚穹頂”的外科手術室里,乙醚的作用如此明顯,到1899年,德國藥理學家漢斯·霍斯特·邁耶,以及1901年英國生物學家查爾斯·歐內斯特·奧弗頓(Charles Ernest Overton)明智地得出結論:脂質溶解度決定了這種麻醉劑的效力。
??漢森回憶說,他在起草一份撥款申請書以進一步調查這一歷史性問題時,曾求助于谷歌搜索,認為他不可能是唯一一個確信膜脂筏作用的人。令漢森高興的是,勒納1997年的PNAS論文中就有關于全麻內源性類似物的假設,麻醉具有如此重要的實際意義,我不敢相信我們不知道所有這些麻醉劑是如何導致人們失去意識的。”
??漢森說,許多其他科學家,通過一個世紀的實驗,已經找到了同樣的答案,但他們缺少幾個關鍵要素:第一,顯微鏡能夠看到比光的衍射極限更小的生物復合體,第二,最近對細胞膜性質的洞察,以及組成它們的多種脂質復合物的復雜組織和功能。
??漢森說:“他們一直在尋找大量的脂質,沒有看到脂質的信號,很大程度上是因為缺乏技術。”。
??漢森實驗室的一位博士后研究人員利用諾貝爾獎獲得者的顯微鏡技術,特別是一種叫做dSTORM的顯微鏡,簡稱“直接隨機光學重建顯微鏡”,漢森解釋說,將細胞浸泡在氯仿中,會大大增加細胞膜脂質簇GM1的直徑和面積。
??漢森說,他所看到的是GM1集群組織的轉變,從擁擠變為一片混亂。當它變得紊亂時,GM1溢出了它的內容物,其中包括一種叫做磷脂酶D2(PLD2)的酶。
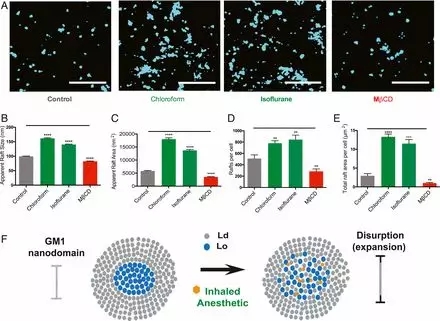
??吸入麻醉藥會破壞GM1域的外觀結構。
??用熒光化學物質標記PLD2,漢森能夠通過dSTORM顯微鏡觀察PLD2像一個臺球一樣從GM1的家移到另一個不太受歡迎的脂質簇PIP2。這激活了PIP2團簇內的關鍵分子,其中包括TREK1鉀離子通道及其脂質激活劑磷脂酸(PA)。漢森說,TREK1的激活基本上凍結了神經元的激活能力,從而導致意識喪失。TREK1鉀離子通道釋放鉀離子,這會使神經產生超極化,更難發射,只能關閉。”。
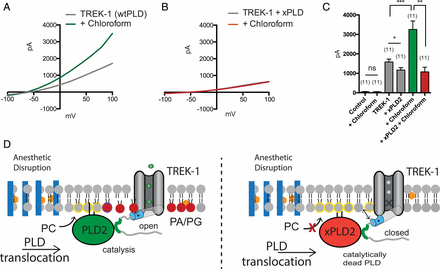
??吸入麻醉劑激活TREK-1取決于PLD2。
??勒納堅持認為他們在活體動物模型中驗證了這一發現。常見的黑腹果蠅提供了這些數據。刪除果蠅中PLD的表達使它們對鎮靜作用產生抵抗。事實上,它們需要兩倍的麻醉劑量才能顯示出同樣的反應。
??他們寫道:“所有的蒼蠅最終都會失去意識,這表明PLD有助于設定一個閾值,但并不是控制麻醉敏感性的唯一途徑。”。
??勒納表示:“人們將開始研究你所能想象到的一切:睡眠、意識、所有那些相關的紊亂。”以太是幫助我們理解意識問題的天賦。它照亮了一條迄今尚未被認識的途徑,大腦顯然已經進化到可以控制更高階的功能。”
